最新の研究
- 2026.04.28
- 瀧ノ上研究室
動く人工細胞の構築を目指した分子コンピューティング技術の開発
人工細胞工学は、分子認識(分子センシング)、情報処理(分子コンピューティング)、自律運動、進化・適応などの細胞が持つ高度な機能を模倣したナノメートル〜マイクロメートルサイズの分子デバイスや分子マシンを構築する研究分野である。近年、合成生物学(Engineering BiologyまたはSynthetic Biologyとも呼ばれる)の分野の中で、化学合成分子や生体分子などの部品をゼロからボトムアップ的に組み上げる、このような人工細胞の構築に注目が集まっている。
人工細胞は、人工的な生体組織や薬物送達システムの構築、薬剤スクリーニング、宇宙・深海探査などにも応用できる環境適応型の自律的スマート材料、マイクロリアクタ、高感度分子センサー、バイオ燃料の生産やバイオ電池、食品バイオテクノロジー向け新材料などの開発、さらには、細胞の機能を再現することによる生命の起源の基礎研究への応用など、様々な分野での利用が期待されている。
現状では、センサーや物質生産といった個々の機能に特化したものが開発されている。将来的には複数の機能を統合したシステムに拡張する必要があるが、そのためには、人工細胞が環境情報をセンシングするだけでなく、分子反応によって自律的に情報処理をして、最終的に、物質生産や人工細胞の動きなど別の機能にその情報処理の結果を伝えるという、分子コンピューティング(分子による情報処理と情報通信)の仕組みが必要となる。
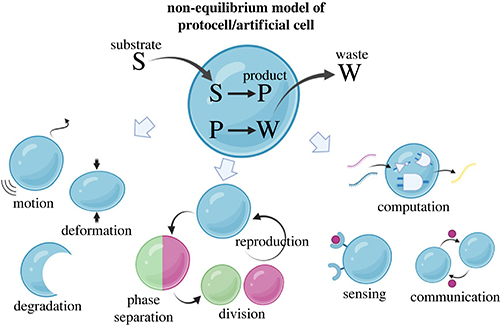
そこで本研究では、分子による情報処理や情報通信が可能な人工細胞の構築を目指した分子コンピューティング技術の開発を進めてきた。この研究では、人工細胞のボディとして、液-液相分離液滴を利用している(Figure 1)(Takinoue, Interface Focus 2023)。液-液相分離液滴は、コアセルベートとも呼ばれ、生命がまだ原始細胞だった頃に存在していた可能性がある分子集合体であり、また、現在の細胞の中にも、膜なしオルガネラとして存在している分子集合体でもある。従来よく研究されてきた分子によるゲルと異なり、液体としての流動性あることが重要で、その性質により、融合や分裂などの動的な振る舞いが出せることが注目されている。
 |
||
| Figure 1. | 相分離液滴を利用した分子コンピューティングシステム | |
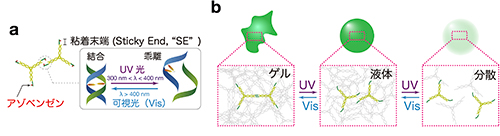
本研究では、刺激により「ゲル」(固い)-「液体」(流動的)-「分散」(溶けている)という相状態の間を可逆的に変化する相分離液滴において、マイクロ流れを実現した。さらにこの相分離液滴のマイクロ流れにより駆動される微小流体ロボットを構築し、その挙動を実証した。相分離液滴は、近年注目されている分岐型DNAナノ構造(3分岐、4分岐、6分岐など)を自己集合させて実現した(Matsuura, Biomacromolecules 2007; Jeon, Soft Matter 2018; Sato, Sci. Adv. 2020)。また、刺激として光(紫外光(UV光)と可視光)を用いた。光刺激によって結合・乖離を行うために分岐型DNAナノ構造の末端にアゾベンゼンを導入している(Figure 2)。このようなアゾベンゼン導入による3分岐DNAナノ構造の自己集合ゲルのゲル化-分散制御による薬剤放出(Kamiya, ChemMedChem 2017)に関してはすでに報告がある。本研究では相分離液滴が示すマイクロスケール流体としてのDNA液滴の流動性の制御に着目し、エネルギーの入力と散逸がもたらす非平衡系における、方向性のある自律運動の観点で研究を行った。
 |
||
| Figure 2. | 光応答性DNA凝集体。(a)光応答性分子を導入した3分岐DNAナノ構造。結合と非結合を光の波長に応じてスイッチできる。(b)光スイッチング(Asanuma, et al. Angew. Chem. Int. Ed. 2001; Kamiya, ChemMedChem 2017)によりDNA凝集体の相状態が変わるため、流動性をコントロールできる。 | |
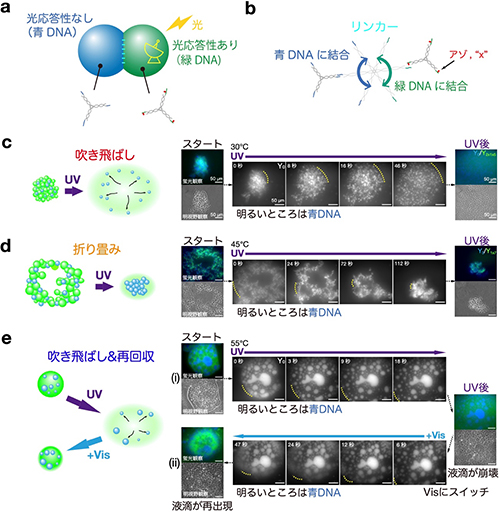
アゾベンゼンの挿入位置、温度、光の照射条件のさまざまな組み合わせを調べた結果、光照射で起こる流れには主に3つのモードがあることが分かった。1つ目のモードでは、UV光照射下で緑DNAゲルが固い「ゲル」状態から急激に「分散」状態へ変化する結果、強い拡散流れが起こり、青DNAゲル粒子を外側に吹き飛ばす(押し出す)ことができる(Figure 3c)。2つ目のモードでは、緑DNAがUV光照射により「ゲル」から「液体」へと変化して流動性を持つようになり、空間的に広がっていた青DNAがコンパクトに折りたたまれるような流れが起こる(Figure 3d)。これは、「ゲル」→「液体」相変化の結果、流体が持つ表面張力的な効果が出現して、全体のボリュームを減らそうとするためである。3つ目のモードでは、液滴の崩壊と再構成が周期的に繰り返すサイクル流れが生じる(Figure 3e)。最初の状態では、緑DNA液滴の中に青DNA液滴が封入されていて、そこにUV光を照射すると、緑DNA液滴が「液体」から「分散」状態へと変化し崩壊し、中の青DNA液滴が放出される。次に可視光に切り替えると、緑DNAは「分散」から「液体」へと戻るため、液滴が再構成されるような流れが生まれる。このような制御は、アゾベンゼン導入DNAのハイブリダイゼーションの自由エネルギー変化の観点で説明することができた。
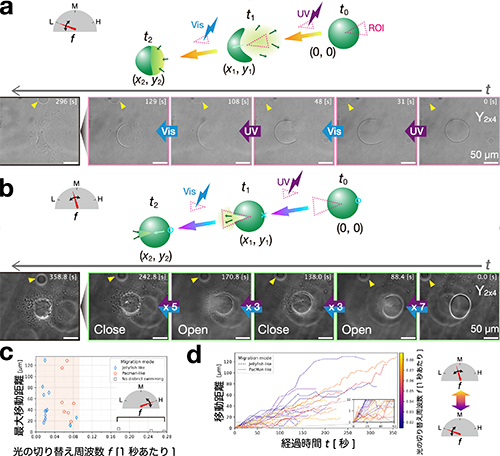
ここまでは、光をDNA凝集体よりも広い領域に照射していたため、対称的な流れ場が生じていた。次に、特殊な装置を使って、DNA液滴の一部だけに照射領域を限定した(Figure 4)。また、波長の切り替え周波数(1秒あたりに何回切り替わるか)を幅広く調べて、その効果を調べた。切り替え周波数が低い場合には、照射領域とは反対側の方向に進むクラゲのような泳動が観察された(Figure 4a)。一方、より高い切り替え周波数では、照射領域と同じ側に向かって、パックマンのように口を開いたり閉じたりしながら進む泳動が見られた(Figure 4b)。切り替え周波数に対して最大移動距離をプロットすると、特定の切り替え周波数を境に「クラゲ」泳動から「パックマン」泳動に切り替わることが分かった(Figures 4c & 4d)。
こうした切り替え周波数依存性を持つ泳動のメカニズムを明らかにするために、モデル化し、数値シミュレーションを行った(Figure 5)。UV光と可視光の切り替えにより、DNAが「液体」と「分散」状態の間をシャトル輸送されるという質量輸送モデルをベースにして、拡散による質量散逸を加味したモデルを構築した。泳動の向き(切り替え周波数を増加させると向きが反転する)、持続時間(周波数が低いほど持続時間が短い)、1ステップあたりの移動幅(周波数が低いほどステップ幅が大きい)に関して、実験結果の傾向と一致するシミュレーション結果が得られた(Figure 5)。このことから、光の切り替え周波数が質量輸送にともなうエネルギーの散逸と交換のバランスを決めていることが明らかとなった。エネルギーの散逸と交換のバランスが切り替わる周波数のしきい値 f をマイクロ流れの拡散係数から見積もったところ、 f ~ 0.07 [s -1]が得られた。この値は、「クラゲ」泳動と「パックマン」泳動が切り替わる周波数領域(Figure 4c)と一致している。
 |
||
| Figure 5. | 計算シミュレーションから泳動のメカニズムを明らかにする。液滴の質量(緑の実線)、速度(オレンジの実線)、位置(ピンクの実線)に着目。光を当てたところと反対の方向がプラス。低い f では質量の減り方が速い→持続時間が短い。光の切り替え周波数 が変わると、移動の向きが反転する。これは実験結果の傾向と一致する。 | |
物理学的には、DNAの凝集のエネルギーの散逸をコントロールすることで得られる、非平衡系における方向性のある自律運動とみなせる点が重要である。このようなシステムを応用する観点からは、今回のインテリジェントな流体は、柔軟なDNAの配列設計や分子修飾を通じて、流体力学的な効果をプログラマブルな作用として操ることができる。例えば、今回構築したDNA液滴のDNA配列に、特定の分子や細胞に特異的にくっつくDNA配列を埋め込めば、泳動しながらターゲットとなる細胞や分子だけを拾いながら、検出、診断、治療などを行うマイクロ流体ロボットが実現できる。また、特定の分子が感知されたときだけ、表面張力的な効果により微小構造物を折り紙のように折りたたむ操作も可能と考えられる。他にも、DNAから構成された人工的な筋肉やポンプなど、機械工学、医療、農業、情報科学などさまざまな分野への応用が期待される。
【参考文献】
Hirotake Udono, Shin-ichiro M. Nomura, Masahiro Takinoue,
"Remote-controlled mechanical and directional motions of photoswitchable DNA condensates",
Nature Communications, 16, 4479, (2025).
DOI: 10.1038/s41467-025-59100-x
「DNA液滴の流動性を光で制御 〜インテリジェントな微小流体型分子コンピュータの実現に期待〜」
2025年6月18日(https://www.isct.ac.jp/ja/news/z436fk2amunb)